Nella SLA non muoiono solo i neuroni: muore anche il sistema di supporto che li tiene in vita. Una ricerca del CIBIO dell’Università di Trento, pubblicata sulla rivista scientifica Brain, ha identificato nella proteina MYC il meccanismo chiave attraverso cui le cellule gliali - quelle deputate a proteggere e nutrire i motoneuroni - si trasformano in elementi dannosi, contribuendo alla degenerazione neurologica.
Come MYC blocca il sistema di supporto ai neuroni
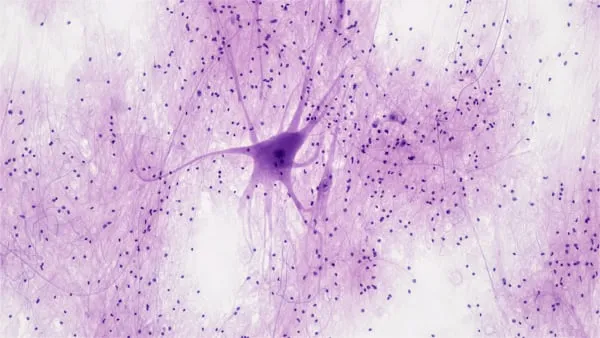
La glia comprende astrociti, oligodendrociti e microglia: cellule non neuronali che svolgono funzioni essenziali come il supporto metabolico ai neuroni, l’eliminazione dei detriti cellulari e la regolazione dell’attività nervosa. In condizioni fisiologiche, gli astrociti rilasciano vescicole extracellulari ricche di fattori trofici che nutrono i neuroni vicini.
Nella SLA questo meccanismo si inceppa. Il gruppo coordinato dalla professoressa Manuela Basso ha osservato che le cellule gliali di pazienti e modelli animali con SLA mostrano un’attivazione anomala della proteina MYC, nota principalmente per il suo ruolo nella proliferazione cellulare. Questa attivazione innesca la gliosi, una risposta reattiva della glia che, anziché proteggere i motoneuroni, li priva del supporto trofico necessario per sopravvivere.
Lo studio ha inoltre dimostrato che l’espressione del TDP-43 mutante negli astrociti è necessaria per innescare la gliosi e le alterazioni comportamentali, individuando un punto d’innesco preciso nella catena causale. Le vescicole extracellulari prodotte dagli astrociti con MYC attivo perdono la funzione trofica e contribuiscono alla neurotossicità: il meccanismo è stato validato su quattro modelli di SLA (TDP-43, SOD1, C9orf72 e SLA sporadica) con cellule, topi e campioni di pazienti. I dettagli metodologici sono nel testo integrale su Brain - Oxford Academic.
Cosa cambia per i 6.000 malati di SLA in Italia
In Italia circa 6.000 persone vivono con la SLA, con 5 nuove diagnosi ogni giorno e oltre 2.000 nuovi casi l’anno. Uno degli aspetti più imprevedibili è la velocità di progressione, che varia enormemente tra un paziente e l’altro: alcuni perdono autonomia in pochi mesi, altri resistono anni. La scoperta di un meccanismo comune tra le diverse forme genetiche e sporadiche della malattia indica un bersaglio condiviso, indipendente dalla mutazione di partenza.
Rilevare i livelli di MYC nelle vescicole extracellulari circolanti potrebbe diventare un biomarcatore prognostico: una misura oggettiva della velocità di progressione, accessibile tramite analisi del liquido cerebrospinale o del sangue. Questo avrebbe ricadute immediate sui trial farmacologici, che oggi faticano a misurare l’efficacia dei trattamenti anche perché arruolano pazienti con decorsi molto diversi. Fondazione AriSLA ha indicato lo sviluppo di biomarcatori per la progressione tra le priorità del Bando 2026, stanziando nel corso degli anni oltre 17 milioni di euro in 121 progetti di ricerca sulla SLA.
Sul fronte terapeutico, se MYC guida il danno nella glia, bloccarlo in modo selettivo apre un percorso farmacologico distinto rispetto agli approcci attuali, orientati soprattutto ai neuroni o alle mutazioni genetiche specifiche. La ricerca sulla conversione delle cellule della pelle in neuroni mostra come la neurobiologia stia esplorando nuove cellule-bersaglio per affrontare malattie un tempo considerate senza alternative terapeutiche.
La ricerca sulla SLA: progressi e incognite
Lo scenario attuale è complesso. Lo studio di fase II su dazucorilant, presentato a fine aprile 2026, ha mancato l’endpoint primario di rallentamento del declino funzionale (scala ALSFRS-R), ma ha mostrato un dato sorprendente: riduzione dell’87% della mortalità a due anni nel gruppo con dosaggio da 300 mg rispetto al placebo (hazard ratio 0,13, p<0,0001). Corcept Therapeutics ha annunciato l’avvio di una fase III entro fine 2026.
La comprensione del ruolo non neuronale nella neurodegenerazione si sta rivelando centrale in molte aree della neurologia: anche la scoperta sul ruolo delle piastrine nella memoria ha mostrato come cellule che non appartengono al sistema nervoso possano influenzare profondamente la funzione cerebrale. La scoperta del CIBIO di Trento non porta ancora un farmaco, ma ridefinisce il bersaglio: per i 6.000 malati di SLA in Italia, sapere dove colpire è il primo passo concreto.
Domande frequenti
Qual è il ruolo della proteina MYC nella SLA secondo lo studio del CIBIO di Trento?
Lo studio ha identificato MYC come meccanismo chiave che induce le cellule gliali a perdere la loro funzione di supporto ai motoneuroni, contribuendo così alla degenerazione neurologica tipica della SLA.
In che modo le cellule gliali diventano dannose nella SLA?
Le cellule gliali, in particolare gli astrociti, attivano in modo anomalo MYC, innescando la gliosi che priva i motoneuroni del supporto trofico e produce vescicole extracellulari neurotossiche.
Perché la scoperta di MYC come bersaglio comune è importante per i malati di SLA?
Individuare un bersaglio comune come MYC, indipendente dal tipo di mutazione, potrebbe permettere lo sviluppo di nuovi trattamenti per tutte le forme di SLA, rendendo la terapia più efficace e personalizzata.
Come potrebbe cambiare la gestione della SLA grazie a questa scoperta?
Rilevare i livelli di MYC nelle vescicole extracellulari potrebbe diventare un biomarcatore prognostico, utile per valutare la progressione della malattia e migliorare la selezione dei pazienti nei trial clinici.
Quali sono le prospettive terapeutiche aperte dalla ricerca sul ruolo di MYC nella SLA?
Bloccare selettivamente MYC nelle cellule gliali apre la strada a strategie farmacologiche innovative, distinte dagli approcci attuali focalizzati sui neuroni o su specifiche mutazioni genetiche.
Lo studio ha già portato a nuove terapie disponibili per i pazienti?
No, la scoperta non ha ancora portato a farmaci disponibili, ma rappresenta un passo importante nell'identificare nuovi bersagli terapeutici e strategie di intervento per la SLA.